7.演習問題
熱力学、特に熱機関(熱サイクル)の問題では、たくさんの物理量が登場し、さらには物理量同士の関係式もたくさん登場する(ボイル、シャルル、状態方程式、熱力学第一法則、モル比熱など)。そのため、実際に問題を見てみても様々な問われ方をして、様々な解き方がある。
しかし、整理して問題を眺めてみると、結局どの問題も似たようなことを聞かれていることが多い。
それゆえ、どのような問題でも対応しやすいように、あらかじめ熱機関の情報を$pV$グラフと前述の表の形にまとめてしまうことが得策であることが多い。(慣れてしまえば情報をまとめる時間はさほどかからず、問題の答えはまとめた情報の中にあることが多い。逆にこのルーティーン化を行わないと、”解き方”の多様さゆえ、熱力学がつかみどころのないもののように感じられてしまうと思われる。)
そこでここでは、まずは今まで学んできたことのポイントをまとめ、その後、熱機関(熱サイクル)の問題を解く際の手順をルーティーン化をしてみたい。
練習問題1 気体の状態変化と熱効率(東京理科大(改))
単原子分子の理想気体の状態を図に示すようなA→B→C→Aの経路に沿って、ゆっくり変化させた。B→Cは等温変化である。

(1)この過程について、次の表に分かる範囲で情報をまとめよ。また、状態Aにおける温度を$T$として、状態A、B、Cにおける温度を$pV$グラフ中に書き込め。
|
|
A⇒B( 変化) |
B⇒C( 変化) |
C⇒A( 変化) |
|
一定になるもの |
|
|
|
|
した仕事 |
|
|
|
|
得た熱量 |
|
|
|
(2)次の各問いに答えよ。
(a) A→Bの過程における気体の内部エネルギーの変化は (1) 〔J〕である。
(b) B→Cの過程において気体が吸収した熱量が$Q$〔J〕であるとすると、気体の内部エネルギーの変化は (2) 〔J〕であり、気体が外部にした仕事は、 (3) 〔J〕である。
(c) C→Aの過程で気体が受けた仕事は、 (4) 〔J〕である。
(d) A→B→C→Aの1サイクルで気体がした正味の仕事は (5) 〔J〕であり、このサイクルの熱効率は、 (6) である。
(3)本問が理想気体の2原子分子であるとすると、(d)の答えはどのように変わるか答えよ。
練習問題2 気体の状態変化と熱効率 断熱変化(愛知教育大学2012(改))
1モルの単原子分子の理想気体が温度$T_0$〔K〕、体積$V_0$〔m3〕、圧力$p_0$〔Pa〕の状態Aにある。図のように、気体の状態がA→B→C→Aの順に変化する過程を考える。過程A→Bは状態Aから気体の体積を一定に保って圧力$3p_0$の状態Bへ変化する過程である。過程B→Cは状態Bから体積$V_c$〔m3〕、圧力$p_0$の状態Cへの断熱変化の過程である。この過程では、気体に出入りする熱量はなく$pV^{5/3}=一定$という関係が成り立つ。過程C→Aは圧力を一定に保って状態Cから状態Aへ変化する過程である。気体定数を$R$〔J/(mol・K)〕とし、過程A→Bにおいて、気体が得る熱量を$Q_{AB}=3RT_0$〔J〕として、各問いに答えよ。ただし、$3^{3/5}=1.93$とする。

(1)この過程について、次の表に情報を分かる範囲でまとめよ。また、各状態A、B、Cにおける温度を$pV$グラフ中に書き込め。
|
|
A⇒B( 変化) |
B⇒C( 変化) |
C⇒A( 変化) |
|
一定になるもの |
|
|
|
|
した仕事 |
|
|
|
|
得た熱量 |
|
|
|
(2)次の各問いに答えよ。
(a) 3つの過程A→B、B→C、C→Aのうち、気体の温度が上昇する過程を全て答えよ。
(b) 過程A→Bにおいて、気体の内部エネルギーの変化量$\Delta U_{AB}$〔J〕を$R$と$T_0$を用いて表せ。
(c) 状態Cの体積$V_c$を$V_0$を用いて表せ。
(d) 過程B→Cにおいて、体積$V$〔m3〕の状態における気体の温度$T$〔K〕を$V$、$T_0$、$V_0$を用いて表せ。
(e) 過程C→Aにおいて、気体が失う熱量$Q_{CA}$〔J〕を$R$と$T_0$を用いて表せ。
(f) 過程A→B→C→Aの1サイクルにおける熱効率$e=W/Q_{AB}$を計算せよ。ここで$W$〔J〕は1サイクルの間に気体が外部にする仕事である。
練習問題 4 気体の状態変化と熱効率
熱機関を利用して上昇、下降するエレベータの熱効率を求めよう。図1のように大気中で鉛直に立てられている底面積$S$〔m2〕の円柱形のシリンダーに質量が無視でき、なめらかに動くピストンがついており、中に単原子分子理想気体が封じこめられている。図1のようにピストンの可動範囲は$h_0$〔m〕から$2h_0$〔m〕までである。重力加速度の大きさを$g$〔m/s2〕とする。
最初、気体の温度が外部の温度と同じ$T_0$〔K〕、気体の圧力$p$が大気圧と同じ$p_0$〔Pa〕、ピストンの高さが$h_0$〔m〕である。このときの状態を状態Aと呼ぶ。
ピストンの上に質量$M$〔kg〕の物体を乗せた。このとき、ピストンは容器の上側に引っ掛かり、ピストンの高さは$h_0$〔m〕のままである。
シリンダー内の気体に熱を与える。しばらく静止し続けた後、ピストンが動きだした。この動きだしたときの状態を状態Bとよぶ。
さらに熱し続けるとゆっくりとピストンは上昇し、高さが$2h_0$〔m〕に達した。このときの状態を状態Cとよぶ。
状態Cになった瞬間に物体をピストンから降ろすとともに熱を与えるのをやめた。ピストンはしばらく静止し続けたが、やがてゆっくりと下降しはじめた。 この下降を始めたときの状態を状態Dと呼ぶ。
下降したピストンは$h_0$〔m〕となったところで静止し、このとき温度は最初の状態Aと同じく$T_0$〔K〕になった。このようにして、この熱機関はサイクルをなす。
〔12弘前大(改)〕

(2)次の各問いに答えよ。
(a) 状態Bのシリンダー内の気体の温度を求めよ。
(b) 状態Aから状態Bまでに気体に与えられた熱量を求めよ。
(c) 状態Cのシリンダー内の気体の温度を求めよ。
(d) 状態Bから状態Cまでに気体に与えられた熱量を求めよ。
(e) 気体の体積を$V$とするとき、このサイクルの$pV$図を図2にかけ。
(f) このサイクルで熱機関が外にした(正味の)仕事を求めよ。
(g) このサイクルの熱効率を求めよ。
(h) $M=\frac{P_0 S}{g}$の場合の熱効率の値を求めよ。
6.ポイントのまとめ
熱力学、特に熱機関(熱サイクル)の問題では、たくさんの物理量が登場し、さらには物理量同士の関係式もたくさん登場する(ボイル、シャルル、状態方程式、熱力学第一法則、モル比熱など)。そのため、実際に問題を見てみても様々な問われ方をして、様々な解き方がある。
しかし、整理して問題を眺めてみると、結局どの問題も似たようなことを聞かれていることが多い。
それゆえ、どのような問題でも対応しやすいように、あらかじめ熱機関の情報を グラフと後述の表の形にまとめてしまうことが得策であることが多い。(慣れてしまえば情報をまとめる時間はさほどかからず、問題の答えはまとめた情報の中にあることが多い。逆にこのルーティーン化を行わないと、”解き方”の多様さゆえ、熱力学がつかみどころのないもののように感じられてしまうと思われる。)
そこでここでは、まずは今まで学んできたことのポイントをまとめ、その後、熱機関(熱サイクル)の問題を解く際の手順をルーティーン化をしてみたい。
1. ポイント
□各状態の気圧$p$ 、体積$V$ 、温度$T$は$pV$グラフ上に表現することができる
□理想気体の状態方程式より、各状態で$pV=nRT$は常に成り立つ
問題文中に$n$、$R$、$T$が与えられていない場合には、$p$、$V$を用いて解答しよう。逆もまたしかり。
□主な状態変化は次の4種類
・定圧変化 圧力一定の変化
・定積変化 体積一定の変化 (つまり 仕事$W_{in}=0$ )
・等温変化 温度一定の変化 (つまり$\Delta U=0$)
・断熱変化 外との熱のやりとりがない変化 (つまり$Q_{in}=0$)
□$pV$グラフの面積は気体がした仕事$W_{out}$を表す
(体積が増えるとき気体がした仕事は正、体積が減るとき気体がした仕事は負)($W_{out}=-W_{in}$)
□内部エネルギーの変化は熱のやり取りによるものと仕事のやり取りの2種類がある。
熱力学の第一法則:$\Delta U=Q_{in}-W_{out}$
□気体の内部エネルギー$U$は温度$T$に比例する
理想気体 単原子分子:$U=\frac{3}{2}nRT$、 2原子分子:$U=\frac{5}{2}nRT$
温度が変わらなければ、内部エネルギーの変化はゼロ
□単原子分子、2原子分子の場合には、定積モル比熱$c_v$、定圧モル比熱$c_p$がそれぞれ次のように表せる。
理想気体 単原子分子:$c_v=\frac{3}{2}R$、$c_p=\frac{5}{2}R$
2原子分子:$c_v=\frac{5}{2}R$、$c_p=\frac{7}{2}R$
(上記以外の場合には$c_v$や$c_p$として問題中に与えられている場合あり)
□状態変化の際に気体が得た熱量はモル比熱から計算するか、熱力学第一法則から計算 することができる。
□熱機関は「どれだけの燃料を用いてどのくらいの仕事をすることができるのか」という効率に関する指標である。
$$熱効率e=\frac{W_{正味のout}}{Q_{in}}=\frac{Q_{in}-Q_{out}}{Q_{in}}$$
2. 各状態変化の特徴
以上のことより、各変化の過程の特徴は次の表ようにまとめることができる。なお、問題を解くときには下の表の灰色部分のみをまとめておこう。また、これらの情報を問題に即した形でまとめるために、モル数、気体の種類(理想気体であるか?単原子分子であるか?2原子分子であるか?)をあらかじめ確認しておこう。
|
|
定積変化 |
定圧変化 |
等温変化 |
断熱変化 |
|
一定になるもの |
P/T=一定 |
V/T=一定 |
PV=一定 |
として、 pVγ=一定 |
|
第一法則の関係 |
Win=0より ΔU=Q |
p=一定より ΔU=Q-pΔV |
温度一定より ΔU=0 |
Q=0より ΔU=Win |
|
した 仕事 |
Wout=0 |
pVグラフの面積より Wout=pΔV |
Wout=Q |
ΔU=-Wout |
|
得た熱量 |
定積モル比熱Cvを用いて Q=nCvΔT (=ΔU) |
定圧モル比熱Cpを用いて Q=nCpΔT |
Q=Wout |
Q=0 |
|
補足 |
単原子分子:Cv=3/2R 2原子分子:Cv=5/2R
|
単原子分子:Cp=5/2R 2原子分子:Cp=7/2R
|
|
ポアソンの法則( として、pVγ=一定)が成り立つ |
|
|
|
|
|
|
【参考】断熱変化におけるポアソンの法則
断熱変化においては、$\gamma=c_p/c_v$として、$pV^\gamma=一定$、もしくは$TV^{\gamma-1}=一定$という関係が成立する。$\gamma$は比熱比と呼ばれ、理想気体 単原子分子の場合には$\gamma=c_p/c_v=\frac{5/2}{3/2}=\frac{5}{3}~1.67$となる。
等温変化では$pV=一定$という関係が成り立つのに対し、断熱変化では$pV^\gamma=一定$($\gamma >1$)が成り立つことから、断熱変化のときの$pV$グラフの傾きは等温変化のグラフよりも急になることが分かる。(下図参照)

熱力学 目次
6.ポイントのまとめ(⇐今ここ!)
5. 分子運動論による理解
気体分子運動論とは、「(気体を微視的・ミクロにとらえ)多数の気体分子が様々な向きに飛び回っているものが気体である」というモデルをもとに気体の性質について考える理論です。この理論によって圧力や温度、エネルギーという様々な巨視的・マクロな物理量同士の関係を説明することができます。つまり、ボイルの法則やシャルルの法則といった経験則が、このモデルを用いて説明できる・理解できるのです。
1.1 このモデルから言えることのまとめ
学び始める前に、このモデルの威力を実感するために、このモデルによって得られる理解をまとめてみます。次のように様々なことがわかります。
・圧力とは多数の気体分子が与える力積の時間平均である。
・温度とは、気体分子の平均の運動エネルギーの程度を表す指標であるといえる。
・理想気体の内部エネルギー(気体が持つエネルギー)は気体分子の運動エネルギーである。
⇒理想気体の内部エネルギーは温度に比例する
・理想気体の比熱は運動エネルギーの自由度に比例する
(単原子分子、2原子分子のモル比熱)
1.2 モデル化の前提
・理想気体を考える。(体積無し、分子間力なし)
・多数の気体分子が様々な向きに飛び回っているものが気体である。
・容器の壁面と気体分子は弾性衝突をする。(分子同士の衝突は無視する)
・衝突時以外は等速直線運動をする。(重力は無視する)
・気体分子は球形をしているとする。(←単原子分子)
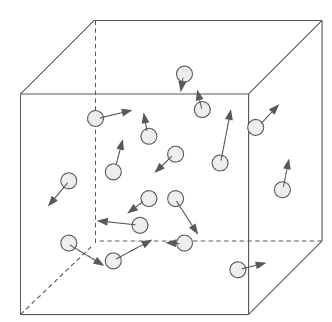
気体はミクロな視点で見ると、たくさんの粒子がバラバラな向きに、バラバラな速さで飛び回っている。
1.3 モデル化
一辺の長さ$L$の立方体の容器に、質量$m$ (kg単位)の気体分子が$N$個入っているものとする。また、図のように座標軸をとる。

(1) $x$方向に動く1分子の衝突が与える力
1個の分子が図のなめらかな壁面Aに$x$方向の速度成分$v_x$で完全弾性衝突したとき、分子の運動量の変化は$-2mv_x$なので、壁面Aに与える力積は$2mv_x$である。この分子は時間$t$の間に$v_x/2L$回壁面Aと衝突するので、この分子によって壁面Aが受ける平均の力の大きさは次のように求められる。
$$\bar{f}=2mv_x \times \frac{v_x}{2L}=\frac{mv_x^2}{L}$$
(2)多数の分子(平均速度$v$)の衝突による圧力の説明
全分子の速度の2乗の平均値$\bar{v^2}$を三平方の定理を用いて各成分の2乗平均値で表すと$\bar{v^2}=\bar{v^2_x}+\bar{v^2_y}+\bar{v^2_z}$であり、等方性より全分子は平均的に$\bar{v^2_x}=\bar{v^2_y}=\bar{v^2_z}$なので、$\bar{v^2}=\bar{v^2_x}+\bar{v^2_y}+\bar{v^2_z}=3 \times \bar{v^2_x}$と表すことができる。前述の平均の力の大きさ$\bar{f}={mv_x^2}/{L}$を用い、$N$個の分子が壁面Aに与える力を、$\bar{v^2}$を用いて書き直すと$\bar{F}=Nm \bar{v^2} / 3L$となる。したがって、壁面Aにはたらく圧力$p$は次のように求まる。
$$p=Nm \bar{v^2} / 3L/L^2=Nm \bar{v^2} / 3V$$
また、$V$を移行して$pv~Nm \bar{v^2} / 3$とするとシャルルの法則が得られる。左辺は巨視的な観測量の積であり、右辺は微視的な分子の運動エネルギーの平均値の合計を表している。つまり、巨視的な経験則である圧力や体積が、微視的な力学的な計算によって導かれているということである。
(3)気体分子モデルによる温度の説明
先に得られた$p=Nm \bar{v^2} / 3V$を、$pV=nRT$を用いて変形すると、次の式が得られる。
$$\frac{1}{2} m \bar{v^2} = \frac{2}{3} \frac{n}{N} RT$$
ここでも、右辺の巨視的な観測量である温度を、左辺の微視的な分子の運動エネルギーの平均値を用いて表している。巨視的な観測量である温度 は実は分子の運動エネルギーの平均値によって決まっていることがわかる。つまり、温度$T$は分子の運動の激しさの指標である。
また、アボガドロ定数$N_A=N/n$を用いて変形すると次式となる。
$$\frac{1}{2}m \bar{v^2} =\frac{2}{3} \frac{1}{N_A} RT$$
これをボルツマンは$k=R/N_A$と置きなおして、次のように表した。
$$\frac{1}{2}m \bar{v^2} =\frac{2}{3} kT$$
この$k$をボルツマン定数と呼ぶ。この式は、$x$、$y$、$z$方向の3方向に対する運動(3自由度)について1方向あたり、$\frac{1}{2}kT$〔J〕のエネルギーが平均として与えられることを示唆している。そして、後に見るように、実際に1自由度あたり$\frac{1}{2}kT$のエネルギーが与えられることが分かっている。このことをエネルギー等分配測という。(のちに、これを利用して5自由度のときの気体のエネルギーを考える。)
(4)気体分子モデルによる気体の内部エネルギー
続いて、気体が持つエネルギーを考える。これを気体の内部エネルギーといい$U$〔J〕で表わす。気体分子運動論では、気体とは多数の気体分子の運動に過ぎないので、エネルギーも多数の気体分子が持っているエネルギーの総和であると考えることができる。
気体粒子が持つエネルギーとは、運動エネルギーと位置エネルギーのみであり、理想気体のように重力や分子間力の影響を無視することができれば、持っているエネルギーは気体分子の運動エネルギーのみとなる。

単原子分子 理想気体の内部エネルギー
運動エネルギーはさらに並進運動と回転運動の二つに分けることができるが、気体分子が球形をしている場合(NeやArなどの希ガスの場合)には、回転運動は無視することができ、並進運動のみを考えれば良くなる。
$N$個の粒子があり、分子の速さの2乗平均が$\bar{v^2}$であるとすると、気体分子のエネルギーの総和は次のように計算できる。
$$U=N \times \frac{1}{2}m\bar{v^2}$$
前述の式$nRT=\frac{1}{3}Nm \bar{v^2}$ より
$$U=\frac{3}{2}nRT$$
この式が理想気体 単原子分子の内部エネルギーを温度で表した式である。また、理想気体であれば、$pV=nRT$は常に成り立つので、$U=\frac{3}{2}nRT =\frac{3}{2} pV$と表すこともできる。ここから、内部エネルギーと温度は比例していることや、1モルの気体の温度を1℃上げると、気体の内部エネルギーは$\frac{3}{2}R$上昇することがわかる。
2原子分子 理想気体の内部エネルギー
上図のような2原子分子(H2やO2などの場合)を考えてみる。このとき、気体分子の運動エネルギーは$x$、$y$、$z$方向の運動の他に、回転によるエネルギーがある。回転の方向は2方向あるため、全体では$x$、$y$、$z$、$x$軸周りの回転、$y$軸周りの回転と、自由度は5になる。前述のエネルギー等分配測を考えると、温度が$T$のとき、各自由度に$\frac{1}{2}kT$ずつエネルギーが与えられるため、内部エネルギーは$U=\frac{5}{2}kT =\frac{5}{2} kT$となる。
ここから、2原子分子の内部エネルギーも温度と比例していることや、1モルの気体の温度を1℃上げると、気体の内部エネルギーは$\frac{5}{2}R$上昇することなどがわかる。
※内部エネルギーと自由度の関係のイメージ:
下図のようないくつかの領域(セル)に区切られている箱を考えよう。それぞれのセルはつながっており、水を入れるとすべてのセルの水は同じ深さになる。ある高さまで水を注ぎたい場合には、セルの数は小さいほど水が早くたまる。逆にセルがたくさんあると、水をそそいでもなかなか深くならない。
気体におけるエネルギー、温度、自由度は、この例における水の量、水深、セルの数の関係に似ている。自由度が3である単原子分子では、セルの数が3つ、自由度が5である2原子分子ではセルの数が5つあることに相当する。エネルギーを注いでも、自由度が大きいと温度が上がりにくく、つまり、比熱が大きいことがわかる。

単原子分子の理想気体 セルの数(自由度)は3 ⇒ $U=3 \times \frac{1}{2}kT=\frac{3}{2}nRT$〔J〕
2原子分子の理想気体 セルの数(自由度)は5 ⇒ $U=5 \times \frac{1}{2}kT=\frac{5}{2}nRT$〔J〕
(5)熱力学第一法則
気体の温度を上昇させるためにはエネルギーを外から加える必要があるが、それには二つの方法がある。1つは気体を加熱することであり、もう1つは外から気体を圧縮するということである。圧縮するということは、外から仕事をすると言い換えることもできる。
加熱するということは、外から熱を加えることによって粒子の平均の運動エネルギーを増加させることであり、気体を圧縮するということは、気体を閉じ込めている壁面が動くことにより1つ1つの気体分子が加速することである。
どちらの方法でも、気体が持つ内部エネルギーが増加するということになるが、エネルギー保存則から気体の内部エネルギーの変化$\Delta U$と与えた熱量$Q_{in}$、気体にした仕事$W_{in}$の間には次の関係が成り立つ。
$$\Delta E = Q_{in} + W_{in}$$
これを熱力学第一法則という。
(6)気体のモル比熱
1 mol の物質を1 K 温度変化させるのに必要な熱を モル比熱( または モル熱容量)という。物質$n$〔mol〕が熱$Q$ 〔J〕を吸収し、温度が$\Delta T$〔K〕上昇するとき、モル比熱をC〔J(/ mol・K)〕とすると、これらの関係は次式で表される。
$$Q=nC\Delta T$$
気体の体積を一定に保ちながら変化させるときのモル比熱を、定積モル比熱$c_v$という。これは、与えた熱量がすべて気体の温度変化に用いられるときの比熱である。
それに対して、気体の圧力を一定に保ちながら変化させるときのモル比熱を 定圧モル比熱 $c_p$ という。圧力が一定の条件下で気体が膨張すると、気体は外に仕事をすることになるので、与えた熱量は気体の温度変化と外への仕事の両方に用いられる。そのため、定圧モル比熱(←体積変化あり)は定積モル比熱(←体積変化なし)よりも大きく(温まりにくく)なる。
具体的には、圧力一定のもとでの外への仕事$W$は、一定の圧力を$p$、体積変化を$\Delta V$として、$W=p \Delta V = nR\Delta T$となるため、体積一定の時と比較すると、$\Delta T$変化させるときには、$nR\Delta T$もしくは$p\Delta V$が余分に必要になる。
よって$nc_p \Delta T = nc_v\Delta T + nR \Delta T$となり$c_p=c_v+R$の関係が得られる(マイヤーの公式)。
単原子分子 理想気体のモル比熱の具体的な計算
前述の$U=\frac{3}{2}nRT$から定積モル比熱を考える。この式より、外に仕事をしない(体積一定の)状態で、理想気体の単原子分子1モル($n$=1)の温度を1℃上昇させるのに必要なエネルギー$c_v$(=定積モル比熱)は$c_v=\frac{3}{2}R$であることがわかる。マイヤーの法則より定圧モル比熱$c_p$は$c_p=c_v+R=\frac{5}{2}R$となる。
2原子分子 理想気体のモル比熱の具体的な計算
単原子分子の2原子分子の場合、内部エネルギーは$U=\frac{5}{2}nRT$であった。この式より、外に仕事をしない(体積一定の)状態で、理想気体の単原子分子1モル($n$=1)の温度を1℃上昇させるのに必要なエネルギー$c_v$(=定積モル比熱)は$c_v=\frac{5}{2}R$であることがわかる。マイヤーの法則より定圧モル比熱 は$c_p=\frac{7}{2}R$となる。
モル比熱 理論値と測定値の比較

※R=8.31程度である
※3R/2=12.465, 5R/2=20.775, 6R/2=24.93
帰結① p=Nmv2/3V ⇒ 圧力とは多数の気体分子が与える力積の時間平均である。
帰結② p=Nmv2/3VよりpV=Nmv2/3=一定 ⇒ シャルルの法則
熱力学 目次
5.気体分子運動モデルによる理解(⇐今ここ!)
【独習】ゼロから 一歩ずつ 物理の見方・考え方 へようこそ
サイト内 記事一覧
|
|
3 運動量保存則とは何か?なぜ、どのような条件で成り立つのか?
たとえば、質量Mの小球(紫)が、質量mの小球(オレンジ)に衝突する例を考えてみましょう。このとき、のちに示すように、二つの小球の運動量の和(←ベクトルとベクトルの和)は、衝突の前後で変化しないことが知られています。運動量の和が保存するということです。これを運動量保存則といいます。

イメージで言うと、衝突前の紫の運動量(の矢印)とオレンジの運動量(の矢印)の和が、衝突後の紫とオレンジの和と等しいということです。
式で表すと次のようになります。
$m\overrightarrow{v}+M\overrightarrow{V}=m\overrightarrow{v'}+M\overrightarrow{V'}$

さらに、これは、2次元を考えても同じことが言えます。例えば、左図のように、平面上を進む紫の小球Aとオレンジの小球Bが衝突した様子を考えましょう。このとき、衝突前のAの運動量とBの運動量の和は、衝突後のAの運動量とBの運動量の和と等しいことが言えます (右図)。


3.1 運動量保存則はなぜ成り立つのか?
運動量保存の法則は、運動方程式と前述の運動量と力積の関係から導くことができます。
例えば簡単のため、先ほどと同じ状況、一直線上を一定の速度𝑉で運動している質量の物体Aが、同じ直線状を一定の速度で運動する質量の物体Bに衝突し、速度がそれぞれ、になる状況を考えてみましょう。衝突の間にBがAから受ける平均の力をとし、衝突時間をとします(右向き正)。

このとき、AがBから受ける平均の力は、BがAから受ける力と作用反作用の関係にありますので、逆向き(逆符号)の-となります。
「物体の運動量の変化は、物体が受けた力積に等しい」を用いて、A、Bそれぞれの運動量の変化は次のように表せます。
式A:$MV'-MV = -F\Delta t$ (下図の上)
式B:$mv'-mv = F\Delta t$ (下図の下)

ここまでくるともう一息、両辺を加えると、A式、B式の右辺が相殺して次式を得ます。
$(MV'-MV)+(mv'-mv) =0$
式変形をすると、求めたい運動量保存則の式が得られます。
$mv+MV=mv'+MV'$
![]()
ぜひ矢印を用いた表記も確認してください。(くどいようですが、運動量はベクトルなので、矢印を用いて表すとイメージが湧きやすいです)。
先ほど紹介した2次元の場合においても、運動量の変化と力積との関係を考えることで、運動量保存則を導いてみましょう。
小球A、小球Bに対する運動量と力積の関係は、矢印の式で表すと次のようになります。
小球A

小球B

これらの二つの式を足し合わせると、右辺の力積が相殺し、次の式が得られます。

移行すると、次のようになります。

これが、すなわち先ほど示した運動量保存の式です。
$mv+MV=mv'+MV'$

3.2 運動量保存則はどのようなときに成り立つのか?
ここで重要な点は、互いに力を及ぼしあう物体同士であったことから、作用反作用の法則により、式A、式Bの右辺($F\Delta t$と$-F\Delta t$)が相殺したということです。つまり運動量保存則が成り立つ条件について、次のことが言えます。
「ある物体系を考えたとき、系に含まれる物体同士の力だけの場合には、物体系の運動量は一定に保たれる。」
この系に含まれる物体同士の力のことを内力、系に含まれない物体からの力を外力と言いますが、この言葉を用いると、次のようにも言い換えることができます。これが良く教科書に載っているいい方です。
「ある物体系を考えたとき、系が外力を受けなければ、物体系の運動量の和は一定に保たれる。」
なお、2次元の例では、上の緑色で示した力積が相殺しているために、運動量保存則が成り立っているということができます。1次元でも2次元でも全く同じように理解することができるはずです。
コラム 「運動量」と「エネルギー」は兄弟?その2
上で、エネルギーと仕事の関係と、運動量と力積の関係を見ました。確かに似ていますが、これだけでは兄弟とは言えないかもしれません。
しかし、実は、これらは生まれもとても似ているのです。
突然ですが、我々は4次元の中に住んでいます。空間3次元と時間1次元です。
改めて仕事$W=\overrightarrow{F} x$と力積$\overrightarrow{I}=\overrightarrow{F}\times \Delta t$をながめてみましょう。どちらも力$\overrightarrow{F}$から生まれています。そしてその力$\overrightarrow{F}$に対して、仕事は空間$\overrightarrow{x}$を掛けており、力積は時間$\Delta t$を掛けているのです(積分という言葉が苦でなければ、仕事は空間で積分しており、力積は時間で積分しているということができます)。
我々が住む4次元のうち、空間を掛けるか(空間で積分するか)、時間を掛けるか(時間で積分するか)という差なのです。いかがでしょうか。兄弟に見えてくるのではないでしょうか。
蛇足ながら、仕事はベクトルとベクトルを掛け算してスカラーになっています。一方で力積はベクトルとスカラーを掛け算してベクトルになっています。それゆえ、仕事やエネルギーはスカラー、一方、力積や運動量はベクトルになるのです。
この兄弟の一番の大きな違いはスカラー、ベクトルの違いだと思います。意識しておいてください。
運動量保存則 目次
2.2.「物体の運動量の変化は、物体が受けた力積に等しい」とはどういうこと?
コラム 「運動量」と「エネルギー」は兄弟?その2(⇐今ここ!)
3.1.運動量保存則はなぜ成り立つのか?
コラム 「運動量」と「エネルギー」は兄弟?その1
「運動量」と「エネルギー」は兄弟のようなものです。
エネルギーと仕事の関係が次のように表されていたことを思い出しましょう。
「物体のエネルギーの変化は、物体がされた仕事に等しい」
これは運動量と力積の関係にとても良く似ています。
「物体の運動量の変化は、物体が受けた力積に等しい」
なお、その導出もとても良く似ています。エネルギーの際には、運動方程式の両辺に$x$を掛けて、右辺を仕事$F\times x$にすることから始めました。
(導出の仕方を思い出そう)
運動方程式の両辺にを掛けて次の式を得ます。
$$ma\times x = F \times x$$
運動の向きに一定の力を受けている物体は等加速度直線運動をするので、公式$v^2-v_0^2 = 2ax$を用いることができます。このの部分を左辺に代入すると、次の式を得ます。
$$m{\frac{v^2-v_0^2}{2}} = F \times x$$
$$\frac{1}{2}mv^2 -\frac{1}{2} v_0^2= F \times x$$
左辺は運動エネルギーの変化、右辺は仕事を表すので、「物体のエネルギーの変化は、物体がされた仕事に等しい」が言えます。
※ここでは、一直線上を運動している物体が一定の力を受ける状況を考えました。
運動量保存則 目次
2.2.「物体の運動量の変化は、物体が受けた力積に等しい」とはどういうこと?
コラム 「運動量」と「エネルギー」は兄弟?その1(⇐今ここ!)
3.1.運動量保存則はなぜ成り立つのか?